來源:網絡
相變材料是指在物質發生相變(通常指一級相變)過程中,可以吸收或釋放大量能量(即相變焓)的一類材料。值得注意的是,在一級相變過程中,理論上溫度是不變的。正是由于相變材料在相變過程中能夠吸收或釋放大量能量,并且溫度保持不變的優異特性,使其在許多工業領域得到了廣泛應用。本文將深入探討潛熱這一關鍵概念,揭示其在相變材料控溫應用中的核心作用,并總結出以下五個觀點。
01 觀點1:相變潛熱是控溫領域的核心力量
相變材料之所以能在工業領域廣泛應用,關鍵在于其獨特的相變潛熱特性。而在相變過程中,每種材料單位質量能吸收或者釋放的熱量,就是我們所說的相變潛熱,單位是J/g。相比之下,通過比熱容計算的顯熱只涉及物質溫度變化時吸收或釋放的熱量,且伴隨著溫度變化,無法實現精準控溫。因此,在控溫領域,相變潛熱才是關鍵,而非顯熱。
02 觀點2:同一物質不同相態變化,潛熱值差異顯著
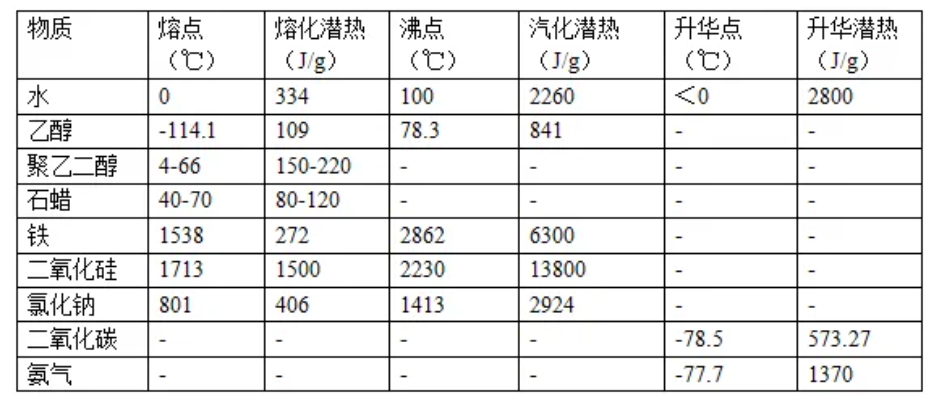
潛熱的大小并非一成不變,同一物質在不同相態變化過程中,潛熱值存在顯著差異。相態的變化一般指的是固態、液態、氣態之間的轉換,液態轉變為氣態(汽化)過程中的潛熱通常要大于固態轉變為液態(熔化)過程中的潛熱。例如,水的熔化潛熱為334 J/g,而汽化潛熱高達2260 J/g,升華潛熱為2800 J/g。顯然,同一種物質的不同相態變化的潛熱大小是顯著不同的,通常情況下:升華潛熱 > 汽化潛熱 > 熔化潛熱。
03 觀點3:不同物質相同相態變化,潛熱值取決于化學鍵和分子間作用力
不同物質即使發生相同的相態變化,其潛熱值也存在顯著差異,這主要取決于物質內部結合方式的不同。物質的構成方式可以分為分子、原子和離子三種,這些不同的構成方式的內部包含了不同的化學鍵。例如,水分子由共價鍵組成,鐵單質由金屬鍵組成,氯化鈉分子由離子鍵組成。此外,即使由相同的化學鍵組成的物質,也存在構成方式的不同性。例如,水是以分子態存在,水分子內部由共價鍵組成,常態下水分子之間是由氫鍵結合的;二氧化硅內部也由共價鍵組成,但二氧化硅不存在獨立的分子,常態下是由硅原子和氧原子以共價鍵形成的網絡結構。與水相比,二氧化硅只存在共價鍵,不存在分子間的氫鍵。
從上述數據可以看出,熔沸點和相變潛熱大小沒有直接關聯性。例如,熔點超過1000℃的鐵的熔化潛熱比熔點在0℃的水的熔化潛熱低,而熔點在801℃的氯化鈉的熔化潛熱比水要高。同樣,以共價鍵組成的水和二氧化硅的熔化潛熱和汽化潛熱差異巨大。04 觀點4:決定物質相變潛熱的因素是在該物質發生相變過程中需要破壞的化學鍵或者分子間作用力所需要的能量大小(鍵能)在這里我們討論的相變是物理過程而非化學過程,而物理變化過程其實是分子或原子間距離發生了改變。決定分子或原子間距離的是分子或原子的結合方式,即之前提到的不同的化學鍵和分子間作用力,以及分子或原子的動能大小。以水為例,固體狀態下,水分子主要以氫鍵結合,每個水分子形成4個氫鍵。而在液體狀態下,由于水分子的運動自由度遠高于固態下,因此平均每個水分子形成的氫鍵少于固態狀態下的4個。同時,液態水分子的動能大于固態下的水分子。因此,可以認為固體水和液體水中氫鍵以及水分子的動能的能量差之和就是水分子的熔化潛熱。同理,氣體水和液體水中氫鍵和水分子的動能能量差就是水分子的汽化潛熱。而氣態水分子之間的力主要是范德華力,幾乎沒有氫鍵的作用。所以我們可以簡單認為,水的熔化以及汽化過程,克服的主要是氫鍵對于水分子的束縛力,水分子內部的共價鍵并沒有遭到破壞。再來看二氧化硅,固態二氧化硅是由硅原子和氧原子通過共價鍵連接形成的網絡狀結構,這種網絡結構非常穩定。液態的二氧化硅中,硅原子和氧原子之間仍然主要通過共價鍵連接,但部分共價鍵已經發生了斷裂,即固態的一個單一網狀結構變成了液態的多個不同的網狀結構。而氣態的二氧化硅是由單個二氧化硅分子組成的,大量的共價鍵在汽化的過程中被破壞。共價鍵的強度遠超氫鍵,因此破壞共價鍵所需要的能量遠超破壞氫鍵所需要的能量。這就解釋了為什么二氧化硅的熔化潛熱和汽化潛熱都比水要大得多。05 觀點5:基于日常使用的溫度區間,影響潛熱的核心變量就是分子間作用力上面我們可以得出結論,決定物質相變潛熱的因素是在該物質發生相變過程中需要破壞的化學鍵或者分子間作用力所需要的能量大小。在這里不討論分子動能了,因為決定動能大小的主要因素是溫度。而討論破壞每種物質的化學鍵所需要的溫度相當于討論該化學鍵的強度大小。從鐵、二氧化硅、氯化鈉的熔沸點可以看到,克服化學鍵的過程是一個高溫過程,克服分子間作用力的過程是一個相對常溫過程。這個溫度區間比較接近我們的日常生活使用場景。因此,在這里僅討論分子間作用力的強弱是由什么決定的。分子間作用力主要有兩種:氫鍵和范德華力。首先讓我們來了解一下什么是氫鍵,氫鍵是由一個氫原子和一個電負性強的原子(如氟、氧、氮)之間的相互作用形成的,通常表示為X-H···Y,其中X和Y是電負性強的原子(如F、O、N),而H是氫原子。還是以水和乙醇為例,之前的內容提到了,乙醇的熔化/汽化潛熱比水小。水分子和乙醇分子的分子間作用力都為氫鍵,且氫鍵均由氫和氧構成,但每個乙醇分子最多可以形成2個氫鍵,而每個水分子最多可以形成4個氫鍵。所以乙醇分子之間的氫鍵比水弱,因此其潛熱值相對較低。進一步可以看到,同樣的氫鍵組成方式依然有決定氫鍵數量的其他因素,這一點值得討論,但這里不做進一步展開了。范德華力是一類分子間或原子間的弱相互作用力,這些力不是由化學鍵(如共價鍵、離子鍵或金屬鍵)產生的,而是由于分子或原子之間的瞬時偶極矩和感應偶極矩引起的。關于偶極矩的定義在此不作展開解釋,我們可以簡單認為分子質量對范德華力有比較大的影響。一般來說,分子質量越大,范德華力就越大,因此潛熱值也越大。例如,戊烷的分子質量為72 g/mol,其熔化潛熱為116 J/g;己烷的分子質量為86 g/mol,其熔化潛熱為151 J/g。在初步了解了潛熱的概念后,我們就可以深入探討相變材料在應用過程中需要注意的其他事項。由于我們在最開始介紹了,相變材料是一種控溫材料,因此我們需要研究的是每種材料發生相變的理論溫度,以及實際使用過程中是否能遵循這個理論發生相變的問題。下一篇我們將研究是什么東西決定了相變材料實際使用過程中的相變溫度和理論的相變溫度之差,即過冷度。
標簽:
導熱界面材料 點擊:
版權聲明:除非特別標注,否則均為本站原創文章,轉載時請以鏈接形式注明文章出處。